![]()
トップ > 倫理審査の申請
倫理審査の申請 Application for Ethics Review
目次
1. 申請に向けての準備
① ユーザー登録<研究者全員必須>
 ←こちらをクリック
←こちらをクリック
申請は「ライフサイエンス研究管理システム」より行います。本システムは「東工大ポータル」のメニュー>各種情報サービス>人を対象とする研究倫理審査申請:[学内限定]にあります。学外から接続される際は「東工大ポータル」のメニュー「学内ネットワークアクセス(SSL-VPN)」からご利用ください。SSL-VPNに初めて接続される方はこちら。
ユーザー登録は一度システムにログインすると自動で行われ、認証に成功するとメインメニューが表示されます。研究に携わる本学の教職員・学生が全員各自でログインしてください。ユーザー登録されていない者を研究者に加えることはできません。
システム申請者向け説明会の動画は、こちら(学内限定)からアクセス可能です。
② 倫理研修を受講 <研究者全員必須>
人を対象とする研究を実施する前に、研究責任者のみならず、学生も含む本学の研究担当者全員が、人を対象とする研究倫理研修を受講する必要があります。詳細はこちら(学内限定)から。
なお、倫理研修のページは学内アクセス限定です。学外から接続される際は「東工大ポータル」のメニュー「学内ネットワークアクセス(SSL-VPN)」からご利用ください。SSL-VPNに初めて接続される方はこちらから。
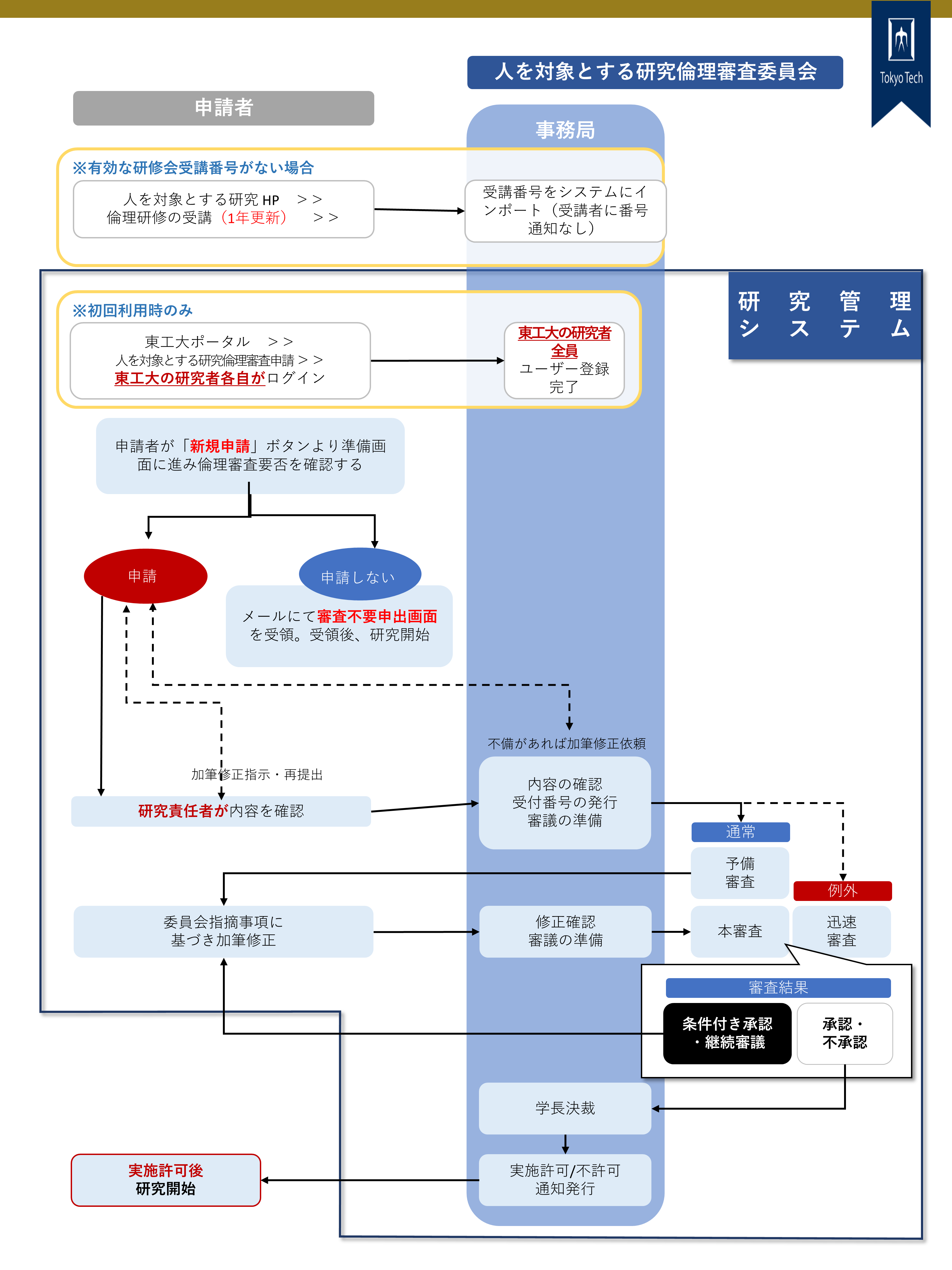
2. 倫理審査要否チェックの実施 <申請者(教員のみ)>
「人を対象とする研究倫理審査申請」メニューから「ライフサイエンス研究管理システム」にて、新規申請ボタンを押下し、倫理審査要否チェックが組み込まれた準備画面 に進みます。必要事項を入力後、研究者等の責務及び倫理的要件の充足を確認し、倫理審査要否チェックを行い、審査該当項目がある場合3-1へ、審査該当項目がない場合は3-2へ、多機関一括審査(本学が分担)の場合は4.へ進みます。
に進みます。必要事項を入力後、研究者等の責務及び倫理的要件の充足を確認し、倫理審査要否チェックを行い、審査該当項目がある場合3-1へ、審査該当項目がない場合は3-2へ、多機関一括審査(本学が分担)の場合は4.へ進みます。
※参考資料 倫理審査要否等チェックリスト "Checklist for Ethics Review Requirement".
"Checklist for Ethics Review Requirement".
※学⽣に審査要否の判断や研究計画・研究内容に責任を負わせることはできないため、教員が倫理審査要否の判断の上、申請や審査不要申出の入力をお願いいたします。
※多機関一括審査済の案件であっても本学の実施許可は必須です。審査ではなく委員長の確認を経て本学学長の実施許可を発行しますので、倫理審査要否チェックでいずれかにチェックをし「倫理審査の申請書を入力する」ボタンを選択してください。
3. 申請・申出 <申請者(教員のみ)>
申請前の留意事項
臨床研究を含む場合
本委員会は医療機関で行われる臨床研究や治験についての審査は行いません。臨床研究等を行う医療機関でまず倫理審査を受け、その審査結果を添えて本委員会に申請を行ってください。本委員会では、本学の研究者が担当する部分(試料・情報の解析等)に限って審査を行います。
侵襲・介入を行う研究の場合
侵襲・介入の有無は申請者による倫理審査要否チェックだけでなく、研究計画書の内容から委員会が個別に判断いたします。
介入研究に該当する場合については、「人を対象とする生命科学・医学系研究に関する倫理指針」に基づき、委員会の許可後、実施に先立ち以下のデータベースに研究を登録する必要があります。研究責任者はご自身の研究が生命科学・医学系倫理指針に該当するか否かを含めて適切な対応をお願いいたします。
厚生労働省:臨床研究実施計画・研究概要公開システム(jRCT)
(参考 「人を対象とする生命科学・医学系研究に関する倫理指針」第3章-第6-4研究の概要の登録)
「人を対象とする研究」における個人情報の取扱い
研究責任者におかれましては、必ず事前に本学個人情報保護規程等関連規則を確認の上、個人情報等の取扱いに誤りの無いよう御注意ください。また、人を対象とする研究倫理審査委員会では、従来クラウド上での個人情報の保管は認めておりませんでしたが、本学が契約しているBoxに限り、①本学認証基盤によるアクセスである。②データセンターが日本国内にある。という二点を鑑み、認めることとなりました。つきましては、Box利用ガイドラインを確認の上、適切な利用をお願いいたします。
国立大学法人東京科学大学個人情報保護規程
ライフサイエンス分野の他の委員会でも審査を必要とする場合
ライフサイエンス分野の他の委員会(遺伝子組換え実験・動物実験・ヒトES細胞・研究用微生物等)
研究内容や実施方法によっては学内の他の委員会でも審査が必要になることがあります。本委員会における審査と同時並行で構いませんので、それぞれの委員会の審査要件を確認の上、必要書類を別途提出して承認を受けてください。
fMRIを利用する研究の場合
設置機関のfMRI安全委員会の確認を受け、審議結果通知(写)を倫理審査システムにアップロードしてください。
利益相反について
研究に営利企業やその他の法人・団体(行政機関、独立行政法人、学校法人を除く)が関わり、医薬品又は医療機器の有効性又は安全性に関する研究等,商業活動に関連し得る研究を実施する場合には,当該研究に係る利益相反に関する状況を把握し,研究計画書に記載しなければなりません。産学共創機構 法務室に最新の人を対象とする倫理審査の申請書を提出し、利益相反マネジメント理工学系審査委員会の確認を受け、審議結果通知(写)を倫理審査システムにアップロードしてください。
※利益相反定期自己申告とは別の申告です。
(参考 利益相反マネジメント理工学系審査委員会 https://www.ori.titech.ac.jp/coi-management/case/03.html )
研究対象者に謝金を支払う場合
研究対象者および実験調査の性質に応じ標準謝金額を定めています。これを超過して謝金を支出する場合は、申請書に超過の理由を記載してください。謝金支出の際は以下の参考をご確認ください。
(参考:経理課「アンケートやモニター(被験者)」への謝金のチェック項目)
傷害保険を利用する場合
人を対象とする研究で発生する万が一の事態に備え、事務局で傷害保険に加入しています。本委員会承認及び学長許可後ご利用いただけます。詳細はこちら。ただし倫理審査不要な研究については、本委員会で契約している傷害保険には加入できませんのでご注意ください。
3-1. 申請の概要(倫理審査要否チェックに該当項目があり、倫理審査の申請書を入力する場合)
■申請要領
必要書類を準備し、新規申請を行います。
(例)本学単独で行う研究の場合
○システムへの入力事項 注釈・記載例入りシステム入力画面(参考)
・申請基本情報
・研究に参加される方への説明書
○システムへの添付書類
・同意書・同意撤回書 
・募集要項 
・関連書類 アンケート、インタビュー聞き取り項目リスト
・実験のイメージ図・写真(市販品なら製造元・型番を記載のこと)
本学単独で行う研究や共同研究などの提出書類一覧はこちらをご参照ください。
■注意事項
・研究開始前に申請してください。(事後審査はいたしません。)
・教員以外が研究計画を立案する場合は、必ず研究責任者が研究計画を確認した上で、申請権限のある教員がシステムへの入力を行ってください。計画作成時には、以下の研究計画書下書き用(Word)をご活用ください。
人を対象とする研究計画書下書き用(日本語) 
Research Protocols involving Human Subjects(for draft)
■提出期限
申請書提出締切日から委員会承認・学長許可まで、1ヶ月半~2ヶ月程度かかります。申請書提出締切日・委員会開催日を確認のうえ、研究を開始したい月の2ヶ月前の締切日に間に合うよう申請してください。
なお、申請書の内容に応じて一部迅速審査を実施しておりますが、迅速審査の該当の有無は、研究内容に拠り委員会が判断します。
■審査結果通知書
審査終了後、本委員会の承認・学長許可を得た後、審査結果通知書を発行いたします。受領後、研究を開始してください。
3-2.審査不要申出の概要(倫理審査要否チェックで該当項目がなく、倫理審査を申請しない場合)
■審査不要申出要領(システム入力画面や様式はこちら)
研究責任者が、「申請者用メニュー」の「新規申請」ボタンを押下し、倫理審査要否チェックが組み込まれた準備画面  に進みます(「閲覧者用メニュー」には新規申請ボタンはありません)。準備画面で「研究者等の責務と倫理的要件の充足を確認した上で、倫理審査を申請しない」ボタンを押下すると、メールにて「審査不要申出確認画面」が届きます。受領後、研究を開始してください。倫理審査不要な研究課題でも、研究対象者に謝金を支出する場合は、審査不要申出を完了しないと支出できません。謝金支出がある場合は,人を対象とする研究計画書(Word)(謝金に関する項目1,2,3,10,11記載必須)と、「審査不要申出画面」を物品等請求システムに添付してください。
に進みます(「閲覧者用メニュー」には新規申請ボタンはありません)。準備画面で「研究者等の責務と倫理的要件の充足を確認した上で、倫理審査を申請しない」ボタンを押下すると、メールにて「審査不要申出確認画面」が届きます。受領後、研究を開始してください。倫理審査不要な研究課題でも、研究対象者に謝金を支出する場合は、審査不要申出を完了しないと支出できません。謝金支出がある場合は,人を対象とする研究計画書(Word)(謝金に関する項目1,2,3,10,11記載必須)と、「審査不要申出画面」を物品等請求システムに添付してください。
■研究実施に際しての留意点
・メールで「審査不要申出確認画面」を受領後、本学実施規則第5条に則り、研究責任者の責務として個人情報の取扱いや研究上の配慮に留意し研究を開始してください。研究対象者向けの説明書や同意書等は以下をご活用ください。
【審査不要申出された方専用】
人を対象とする研究計画書(日本語) 
Research Protocols involving Human Subjects 
説明書 
同意書・同意撤回書 
募集要項 
4.多機関一括審査(本学が分担)<申請者(教員のみ)>
多機関一括審査済の案件であっても本学の実施許可は必須です。研究代表者の所属する研究機関で一括審査を受審し、許可を得た後、本学では審査ではなく委員長の確認を経て学長の実施許可を発行します。研究課題名冒頭に【多機関一括審査済】と入力し、申請してください。システムへの入力方法と提出書類につきましては、(記載例)多機関一括審査済  をご参照ください。
をご参照ください。
【ご参考】多機関一括審査の際に求められる情報について
多機関一括審査に際し、一括審査を実施する機関から、本学倫理審査委員会に関しての情報が求められる場合がございます。よくあるお問い合わせ内容につきましては多機関一括審査に関するQ&Aをご参照ください。
5.研究計画変更<申請者(教員のみ)>
既に許可を受けている研究計画を変更する場合には、事前に変更申請を行い、承認・許可を受けてください。
システム改修により変更申請書へ「4.倫理審査要否チェック」が組み込まれました。改めてチェックをお願いいたします。新たな実験の追加等の「研究方法の変更」は変更申請ではなく新規申請をお願いいたします。
<チェック項目がある場合>
変更申請を行ってください。申請者権限が教員に限定されたため、過去に学生が申請した課題を変更する場合は研究責任者から行って下さい。(システム入力画面や様式はこちら)
<チェック項目がない場合>
倫理審査要否チェックを行い、特に倫理的配慮が必要ないと判断した場合は、終了報告を提出し、新たに審査不要申出を行ってください。終了報告には以下を記載ください。
※「規則改訂により、倫理審査委員会での審査が不要となったため、終了報告を提出します。なお、研究は継続して行なっているため、研究タイトルと研究担当者・研究期間を記載した審査不要申出を提出します。」
6.報告書<申請者(教員のみ)>
倫理指針に定める通り研究を継続して実施する場合や終了や中止をする場合には、「ライフサイエンス研究管理システム」上で報告書を提出ください。「研究課題一覧」から対象となる研究課題を表示し、報告書の種類を選んでください。(システム入力画面や様式はこちら)
6-1.実施状況報告
毎年2月~3月初に報告書提出を依頼する通知が届きますので、翌年度も研究期間が残っている課題についてシステムから実施状況報告をご提出ください。
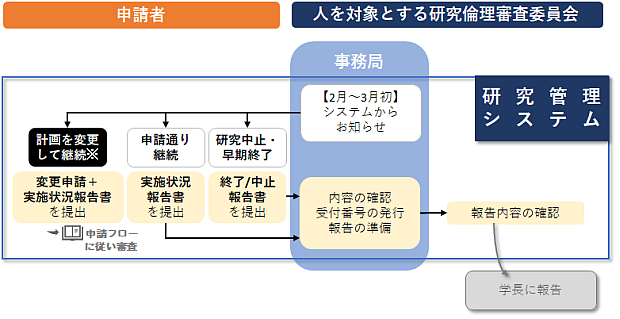
6-2.終了・中止報告
研究が終了した時、研究を中止した時には報告を行ってください
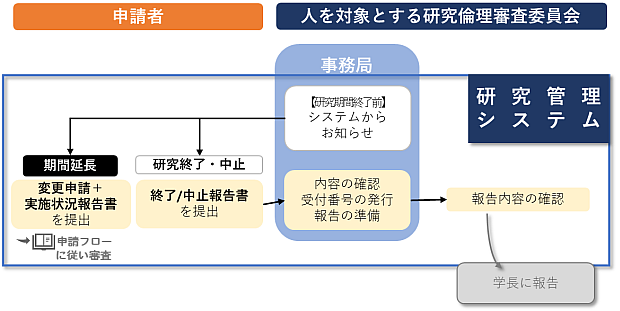
6-3.有害事象報告
事故や、研究対象者の健康や安全もしくは研究継続に影響する事象が発生した/する可能性がある場合には、速やかに報告を行ってください。
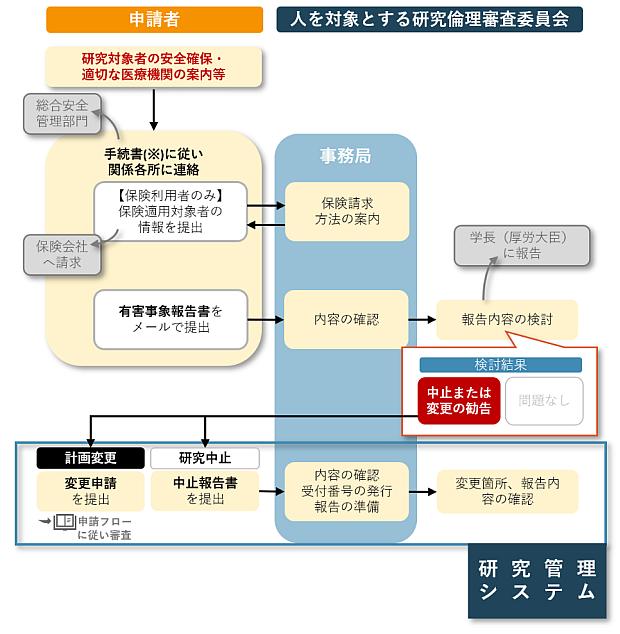
※人を対象とする研究に関する業務手順書参照
※キャンパスマネジメント本部総合安全管理部門(事件・事故等)
7.申請フロー